A tüdőtranszplantáció az előrehaladott tüdőbetegség elfogadott kezelési módja. Az elmúlt évtizedekben a tüdőtranszplantáció figyelemre méltó előrelépést tett a transzplantált betegek szűrésében és értékelésében, a donor tüdők kiválasztásában, megőrzésében és elosztásában, a sebészeti technikákban, a posztoperatív ellátásban, a szövődmények kezelésében és az immunszuppresszióban.
Több mint 60 év alatt a tüdőtranszplantáció a kísérleti kezelésből az életveszélyes tüdőbetegségek elfogadott standard kezelésévé fejlődött. Az olyan gyakori problémák ellenére, mint az elsődleges graft diszfunkció, a krónikus transzplantációs tüdő diszfunkció (CLAD), az opportunista fertőzések fokozott kockázata, a rák és az immunszuppresszióval összefüggő krónikus egészségügyi problémák, ígéretes a betegek túlélésének és életminőségének javítása a megfelelő recipiens kiválasztásával. Míg a tüdőtranszplantációk egyre gyakoribbak világszerte, a műtétek száma még mindig nem tart lépést a növekvő igényekkel. Ez az áttekintés a tüdőtranszplantáció jelenlegi állapotára és a legújabb eredményekre, valamint a kihívásokkal teli, de potenciálisan életet megváltoztató terápia hatékony megvalósításának jövőbeli lehetőségeire összpontosít.
A potenciális kedvezményezettek értékelése és kiválasztása
Mivel a megfelelő donor tüdők viszonylag ritkák, a transzplantációs központoknak etikailag kötelező a donor szerveket olyan potenciális recipienseknek kiosztani, akiknél a legnagyobb a valószínűsége a transzplantációból származó nettó haszonnak. Az ilyen potenciális recipiensek hagyományos meghatározása szerint becslések szerint több mint 50%-os a kockázata annak, hogy 2 éven belül tüdőbetegségben meghalnak, és több mint 80%-os az esélye annak, hogy 5 évig túlélik a transzplantációt, feltételezve, hogy az átültetett tüdők teljesen működőképesek. A tüdőtranszplantáció leggyakoribb indikációi a tüdőfibrózis, a krónikus obstruktív tüdőbetegség, a tüdőérbetegség és a cisztás fibrózis. A betegeket a csökkent tüdőfunkció, a csökkent fizikai funkció és a betegség progressziója alapján utalják be a gyógyszeres és sebészeti terápiák maximális alkalmazása ellenére; más betegségspecifikus kritériumokat is figyelembe vesznek. A prognosztikai kihívások támogatják a korai beutalási stratégiákat, amelyek lehetővé teszik a jobb kockázat-haszon tanácsadást a megalapozott közös döntéshozatal javítása és a sikeres transzplantációs eredmények lehetséges akadályainak megváltoztatásának lehetősége érdekében. A multidiszciplináris csapat felméri a tüdőtranszplantáció szükségességét és a beteg immunszuppresszánsok alkalmazása miatti transzplantáció utáni szövődményeinek kockázatát, például a potenciálisan életveszélyes fertőzések kockázatát. Kritikus fontosságú a tüdőn kívüli szervkárosodás, a fizikai erőnlét, a mentális egészség, a szisztémás immunitás és a rák szűrése. A koszorúerek és agyi artériák, a vesefunkció, a csontok egészsége, a nyelőcsőfunkció, a pszichoszociális kapacitás és a szociális támogatás specifikus vizsgálata, miközben ügyelnek az átláthatóság fenntartására, hogy elkerüljék az egyenlőtlenségeket a transzplantációra való alkalmasság meghatározásakor.
Több kockázati tényező károsabb, mint az egyes kockázati tényezők. A transzplantáció hagyományos akadályai közé tartozik az előrehaladott életkor, az elhízás, a rákos megbetegedések kórtörténete, a kritikus betegség és az egyidejűleg fennálló szisztémás betegségek, de ezeket a tényezőket a közelmúltban megkérdőjelezték. A recipiensek életkora folyamatosan növekszik, és 2021-re az Egyesült Államokban a recipiensek 34%-a 65 év feletti lesz, ami azt jelzi, hogy a biológiai életkor egyre nagyobb hangsúlyt kap a kronológiai életkorral szemben. Manapság a hatperces gyaloglási távolság mellett gyakran hivatalosabb értékelést is végeznek a törékenységről, amely a fizikai tartalékokra és a stresszorokra adott várható válaszokra összpontosít. A törékenység a tüdőtranszplantáció utáni rossz eredményekkel jár, és a törékenység általában a testösszetétellel függ össze. Az elhízás és a testösszetétel kiszámítására szolgáló módszerek folyamatosan fejlődnek, kevésbé a BMI-re, és inkább a zsírtartalomra és az izomtömegre összpontosítanak. Olyan eszközöket fejlesztenek, amelyek ígéretet tesznek a tétovázás, az oligomiózis és a rugalmasság számszerűsítésére, hogy jobban megjósolják a tüdőtranszplantáció utáni felépülési képességet. A műtét előtti tüdőrehabilitációval lehetőség van a testösszetétel és a legyengültség módosítására, ezáltal javítva az eredményeket.
Akut kritikus betegség esetén különösen nehéz meghatározni a legyengültség mértékét és a felépülési képességet. A gépi lélegeztetésben részesülő betegeknél korábban ritkák voltak a transzplantációk, de most egyre gyakoribbak. Ezenkívül az elmúlt években megnőtt az extrakorporális életfenntartás alkalmazása transzplantáció előtti átmeneti kezelésként. A technológia és az érrendszeri hozzáférés fejlődése lehetővé tette, hogy az éber, gondosan kiválasztott, extrakorporális életfenntartásban részesülő betegek részt vegyenek a tájékoztatáson alapuló beleegyezési eljárásokban és a fizikai rehabilitációban, és a transzplantáció után hasonló eredményeket érjenek el, mint azok a betegek, akiknek a transzplantáció előtt nem volt szükségük extrakorporális életfenntartásra.
A kísérő szisztémás betegséget korábban abszolút ellenjavallatnak tekintették, de a transzplantáció utáni kimenetelre gyakorolt hatását mostantól külön kell értékelni. Tekintettel arra, hogy a transzplantációval összefüggő immunszuppresszió növeli a rák kiújulásának valószínűségét, a meglévő rosszindulatú daganatokra vonatkozó korábbi irányelvek hangsúlyozták azt a követelményt, hogy a betegeknek öt évig rákmentesnek kell lenniük, mielőtt transzplantációs várólistára kerülnének. Azonban, ahogy a rákterápiák hatékonyabbá válnak, most már ajánlott a rák kiújulásának valószínűségét betegenként egyedileg felmérni. A szisztémás autoimmun betegségeket hagyományosan ellenjavalltnak tekintették, ez a nézet pedig problematikus, mivel az előrehaladott tüdőbetegség általában korlátozza az ilyen betegek várható élettartamát. Az új irányelvek azt javasolják, hogy a tüdőtranszplantációt célzottabb betegségfelmérés és kezelés előzze meg, hogy csökkentsék azokat a betegségtüneteket, amelyek hátrányosan befolyásolhatják a kimeneteleket, például a szklerodermával összefüggő nyelőcsőproblémákat.
A specifikus HLA-alosztályok elleni keringő antitestek egyes potenciális recipienseket allergiássá tehetnek bizonyos donor szervekre, ami hosszabb várakozási időt, a transzplantáció valószínűségének csökkenését, akut szervkilökődést és a CLAD fokozott kockázatát eredményezi. Azonban egyes, a recipiensre specifikus antitestekkel és donortípusokkal végzett transzplantációk hasonló eredményeket értek el műtét előtti deszenzitizációs kezelésekkel, beleértve a plazmacserét, az intravénás immunglobulin adagolását és az anti-B-sejt terápiát.
Donor tüdő kiválasztása és alkalmazása
A szervadományozás önzetlen cselekedet. A donor beleegyezésének megszerzése és autonómiájának tiszteletben tartása a legfontosabb etikai tényezők. A donor tüdejét károsíthatja mellkasi trauma, újraélesztés, aspiráció, embólia, lélegeztetőgéppel összefüggő sérülés vagy fertőzés, illetve neurogén sérülés, ezért sok donor tüdő nem alkalmas transzplantációra. ISHLT (Nemzetközi Szív- és Tüdőátültetési Társaság)
A tüdőtranszplantáció általánosan elfogadott donorkritériumokat határoz meg, amelyek transzplantációs központonként eltérőek. Valójában nagyon kevés donor felel meg a tüdőadományozás „ideális” kritériumainak (2. ábra). A donor tüdők fokozott felhasználását a donorkritériumok enyhítésével (azaz olyan donorok, akik nem felelnek meg a hagyományos ideális szabványoknak), gondos értékeléssel, aktív donorgondozással és in vitro értékeléssel érték el (2. ábra). A donor aktív dohányzása a recipiens primer graft diszfunkciójának kockázati tényezője, de az ilyen szervek felhasználásából eredő halálozás kockázata korlátozott, és mérlegelni kell a soha nem dohányzó donor tüdejére való hosszú várakozás halálozási következményeivel szemben. Az idősebb (70 évnél idősebb) donoroktól származó, szigorúan kiválasztott és egyéb kockázati tényezőkkel nem rendelkező tüdő felhasználása hasonló recipiens túlélési és tüdőfunkciós eredményeket érhet el, mint a fiatalabb donoroktól származók esetében.
A több szervdonor megfelelő ellátása és a tüdőadományozás lehetőségének mérlegelése elengedhetetlen annak biztosításához, hogy a donor tüdők nagy valószínűséggel alkalmasak legyenek a transzplantációra. Bár a jelenleg rendelkezésre álló tüdők közül kevés felel meg az ideális donor tüdő hagyományos definíciójának, a kritériumok ezen hagyományos kritériumokon túli enyhítése a szervek sikeres felhasználásához vezethet az eredmények veszélyeztetése nélkül. A tüdőmegőrzés standardizált módszerei segítenek megvédeni a szerv integritását, mielőtt azt beültetnék a recipiensbe. A szervek különböző körülmények között szállíthatók transzplantációs intézményekbe, például kriosztatikus tartósítással vagy mechanikus perfúzióval hipotermiában vagy normál testhőmérsékleten. Azok a tüdők, amelyeket nem tartanak alkalmasnak azonnali transzplantációra, további objektív értékelésnek vethetők alá, és in vitro tüdőperfúzióval (EVLP) kezelhetők, vagy hosszabb ideig tartósíthatók a transzplantáció szervezési akadályainak leküzdése érdekében. A tüdőtranszplantáció típusa, az eljárás és az intraoperatív támogatás mind a beteg igényeitől, valamint a sebész tapasztalatától és preferenciáitól függ. Azoknál a potenciális tüdőtranszplantált recipienseknél, akiknek betegsége drámaian romlik a transzplantációra való várakozás alatt, az extrakorporális életmentés mérlegelhető transzplantáció előtti átmeneti kezelésként. A korai posztoperatív szövődmények közé tartozhat a vérzés, a légutak elzáródása vagy az érrendszeri anasztomózis, valamint a sebfertőzés. A mellkasban található rekeszizom vagy vagus ideg károsodása egyéb szövődményekhez vezethet, amelyek befolyásolhatják a rekeszizom működését, illetve a gyomor kiürülését. A donor tüdőben a beültetés és a reperfúzió után korai akut tüdőkárosodás, azaz primer graft diszfunkció alakulhat ki. Érdemes osztályozni és kezelni a primer graft diszfunkció súlyosságát, amely a korai halálozás magas kockázatával jár. Mivel a potenciális donor tüdőkárosodás a kezdeti agysérülést követő órákon belül jelentkezik, a tüdő ellátásának magában kell foglalnia a megfelelő lélegeztetési beállításokat, az alveoláris reexpanziót, a bronchoszkópiát és aspirációt, valamint a lavaget (a tenyészetek mintavételéhez), a beteg folyadékkezelését és a mellkas helyzetének beállítását. Az ABO az A, B, AB és O vércsoportot, a CVP a centrális vénás nyomást, a DCD a szívhalálból származó tüdődonort, az ECMO az extrakorporális membrán oxigenizációt, az EVLW az extravaszkuláris tüdővizet, a PaO2/FiO2 az artériás parciális oxigénnyomás és a belélegzett oxigénkoncentráció arányát, a PEEP pedig a pozitív kilégzésvégi nyomást jelenti. A PiCCO a pulzusindex hullámforma szívteljesítményét jelöli.
Egyes országokban a kontrollált donor tüdő (DCD) alkalmazása 30-40%-ra emelkedett a szívhalálozással járó betegeknél, és hasonló akut szervkilökődési, CLAD- és túlélési arányokat értek el. Hagyományosan kerülni kell a fertőző vírussal fertőzött donoroktól származó szervek nem fertőzött recipiensekbe történő átültetését; Az elmúlt években azonban a hepatitis C vírus (HCV) ellen közvetlenül ható vírusellenes gyógyszerek lehetővé tették a HCV-pozitív donor tüdők biztonságos átültetését HCV-negatív recipiensekbe. Hasonlóképpen, humán immundeficiencia vírus (HIV) pozitív donor tüdők átültethetők HIV-pozitív recipiensekbe, és hepatitis B vírus (HBV) pozitív donor tüdők átültethetők HBV ellen oltott és immunis recipiensekbe. Jelentések érkeztek aktív vagy korábban SARS-CoV-2-vel fertőzött donorokból származó tüdőátültetésekről. További bizonyítékokra van szükségünk annak meghatározásához, hogy biztonságos-e a donor tüdők fertőző vírusokkal történő átültetése transzplantáció céljából.
A több szerv kinyerésének összetettsége miatt nehéz felmérni a donor tüdők minőségét. Az in vitro tüdőperfúziós rendszer használata lehetővé teszi a donor tüdőfunkciójának és a felhasználás előtti helyreállítás lehetőségének részletesebb értékelését (2. ábra). Mivel a donor tüdő nagyon érzékeny a sérülésekre, az in vitro tüdőperfúziós rendszer platformot biztosít specifikus biológiai terápiák beadásához a sérült donor tüdő helyreállítására (2. ábra). Két randomizált vizsgálat kimutatta, hogy a hagyományos kritériumoknak megfelelő donor tüdők in vitro normál testhőmérsékletű tüdőperfúziója biztonságos, és hogy a transzplantációs csapat így meghosszabbíthatja a tartósítási időt. A donor tüdők magasabb hipotermián (6-10°C) történő, jégen történő tartósítása a 0-4°C-os tárolás helyett javítja a mitokondriális egészséget, csökkenti a károsodást és javítja a tüdőfunkciót. A félig szelektív nappali transzplantációk esetében a hosszabb éjszakai tartósításról számoltak be, hogy jó transzplantáció utáni eredményeket lehet elérni. Jelenleg folyamatban van egy nagyszabású, nem rosszabb biztonsági vizsgálat, amely a 10°C-on történő tartósítást hasonlítja össze a standard krioprezervációval (regisztrációs szám: NCT05898776 a ClinicalTrials.gov oldalon). Az emberek egyre inkább a mielőbbi szervgyógyítást szorgalmazzák a több szervet befogadó donorközpontokon keresztül, és a szervfunkciók javítását szervjavító központokon keresztül, hogy jobb minőségű szerveket lehessen felhasználni transzplantációhoz. Ezen változások hatását a transzplantációs ökoszisztémában még mindig értékelik.
A kontrollálható DCD szervek megőrzése érdekében a normál testhőmérséklet lokális in situ perfúziója extrakorporális membrán oxigenizációval (ECMO) alkalmazható a hasi szervek működésének felmérésére, valamint a mellkasi szervek, köztük a tüdő közvetlen megszerzésének és megőrzésének támogatására. A mellkasban és a hasban a normál testhőmérséklet lokális perfúziója utáni tüdőtranszplantációval kapcsolatos tapasztalatok korlátozottak, és az eredmények vegyesek. Aggodalomra ad okot, hogy ez az eljárás károsíthatja az elhunyt donorokat, és sértheti a szervgyűjtés alapvető etikai elveit; Ezért a normál testhőmérsékleten végzett lokális perfúzió sok országban még nem engedélyezett.
Rák
A tüdőtranszplantáció utáni populációban a rákos megbetegedések előfordulása magasabb, mint az átlagnépességben, és a prognózis általában rossz, a halálesetek 17%-át teszi ki. A tüdőrák és a transzplantáció utáni limfoproliferatív betegség (PTLD) a rákkal összefüggő halálozás leggyakoribb okai. A hosszú távú immunszuppresszió, a korábbi dohányzás hatásai vagy az alapbetegség kockázata mind hozzájárul a tüdőrák kialakulásának kockázatához egyetlen tüdőrecipiens saját tüdejében, de ritka esetekben donor által átvitt szubklinikai tüdőrák is előfordulhat transzplantált tüdőben. A nem-melanoma bőrrák a leggyakoribb rák a transzplantált betegek körében, ezért a bőrrák rendszeres monitorozása elengedhetetlen. Az Epstein-Barr vírus által okozott B-sejtes PTLD a betegség és a halálozás fontos oka. Bár a PTLD minimális immunszuppresszióval is megszűnhet, általában rituximabbal, szisztémás kemoterápiával vagy mindkettővel végzett B-sejtes célzott terápiára van szükség.
Túlélés és hosszú távú eredmények
A tüdőtranszplantáció utáni túlélés továbbra is korlátozott más szervátültetésekhez képest, átlagosan 6,7 évvel, és a betegek hosszú távú eredményeiben három évtized alatt kevés előrelépés történt. Sok beteg azonban jelentős javulást tapasztalt az életminőségben, a fizikai állapotban és egyéb, a betegek által jelentett eredményekben; A tüdőtranszplantáció terápiás hatásainak átfogóbb értékelése érdekében nagyobb figyelmet kell fordítani az ezen betegek által jelentett eredményekre. Fontos kielégítetlen klinikai igény a recipiens halálának kezelése a késleltetett graft-elégtelenség vagy a hosszan tartó immunszuppresszió halálos szövődményei miatt. A tüdőtranszplantáción átesett betegek számára aktív, hosszú távú ellátást kell biztosítani, amely csapatmunkát igényel a recipiens általános egészségének védelme érdekében egyrészt a graft funkciójának monitorozásával és fenntartásával, másrészt az immunszuppresszió káros hatásainak minimalizálásával, valamint a recipiens fizikai és mentális egészségének támogatásával (1. ábra).
Jövőbeli irány
A tüdőtranszplantáció egy olyan kezelés, amely rövid idő alatt sokat fejlődött, de még nem érte el teljes potenciálját. A megfelelő donor tüdők hiánya továbbra is komoly kihívást jelent, és még mindig fejlesztés alatt állnak a donorok felmérésére és ellátására, a donor tüdők kezelésére és helyreállítására, valamint a donorok megőrzésének javítására szolgáló új módszerek. A nettó haszon további növelése érdekében javítani kell a szervelosztási politikákat a donorok és a recipiensek közötti párosítás javításával. Egyre nagyobb az érdeklődés a kilökődés vagy fertőzés molekuláris diagnosztika útján történő diagnosztizálása iránt, különösen a donortól származó szabad DNS-sel, vagy az immunszuppresszió minimalizálásának irányítása iránt; Azonban ezen diagnosztikai módszerek hasznossága a jelenlegi klinikai graftmonitorozási módszerek kiegészítéseként még meghatározásra vár.
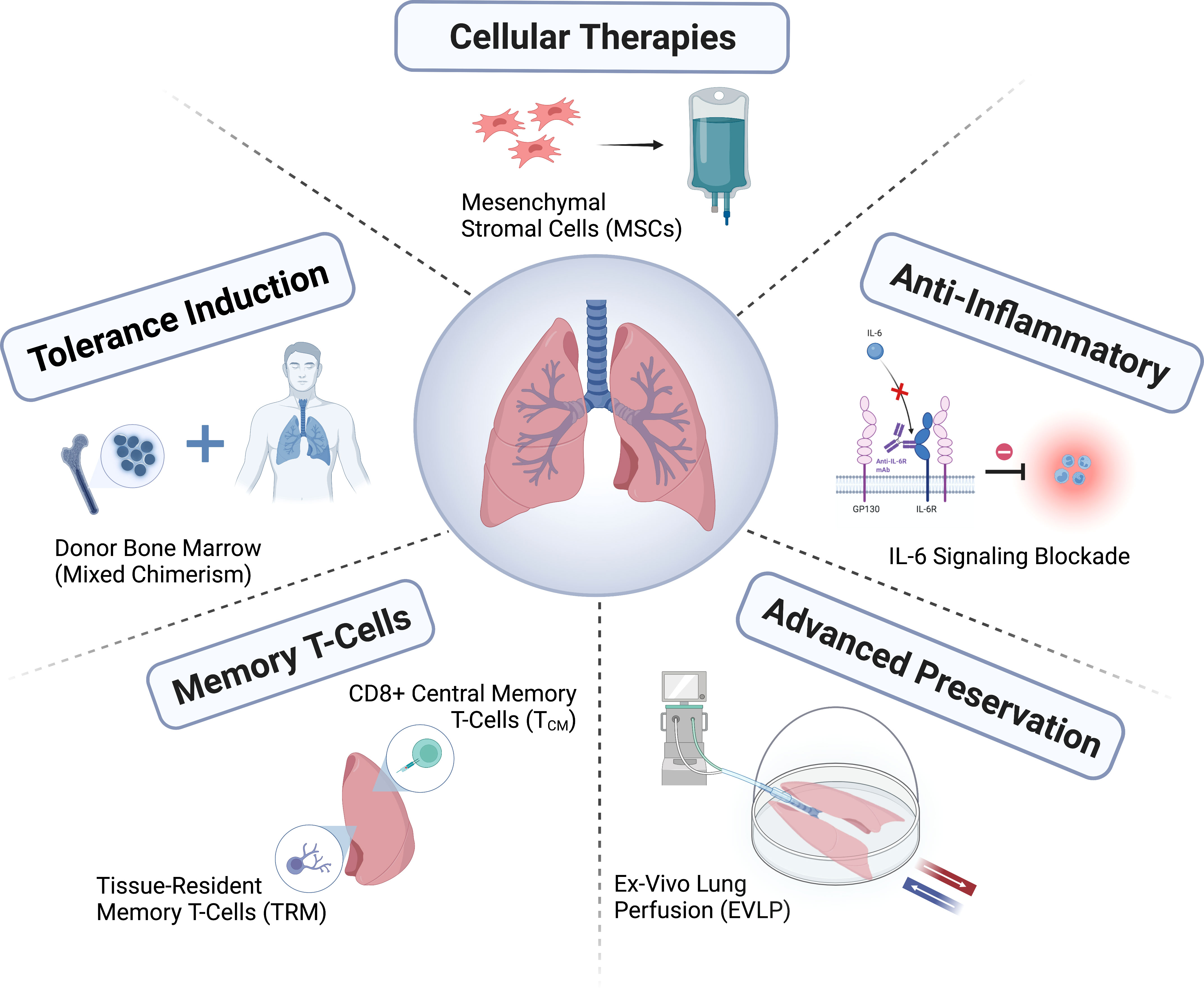
A tüdőtranszplantáció területe konzorciumok (pl. ClinicalTrials.gov regisztrációs szám: NCT04787822; https://lungtransplantconsortium.org) létrehozásával fejlődött ki, amelyek lehetővé teszik az együttműködést, elősegítik a primer graft diszfunkció megelőzését és kezelését, a CLAD előrejelzését, a korai diagnózist és a belső pontok (endotipizálás) meghatározását, a finomító szindrómát. Gyorsabb előrelépés történt a primer graft diszfunkció, az antitest-közvetített kilökődés, az ALAD és a CLAD mechanizmusok vizsgálatában. A mellékhatások minimalizálása és az ALAD és a CLAD kockázatának csökkentése személyre szabott immunszuppresszív terápiával, valamint a betegközpontú eredmények meghatározása és beépítése az eredménymutatókba kulcsfontosságú lesz a tüdőtranszplantáció hosszú távú sikerének javításához.
Közzététel ideje: 2024. november 23.