Napjainkban az alkoholmentes zsírmájbetegség (NAFLD) a krónikus májbetegségek fő okává vált Kínában és az egész világon. A betegségspektrum magában foglalja az egyszerű máj steatohepatitist, a nem alkoholos steatohepatitist (NASH) és a kapcsolódó cirrózist és májrákot. A NASH-t a hepatocitákban felhalmozódott túlzott zsír, valamint az indukált sejtkárosodás és gyulladás jellemzi, májfibrózissal vagy anélkül. A NASH-betegek májfibrózisának súlyossága szorosan összefügg a rossz májprognózissal (cirrózis és szövődményei, valamint májsejtes karcinóma), a szív- és érrendszeri eseményekkel, az extrahepatikus rosszindulatú daganatokkal és a bármilyen okból bekövetkező halállal. A NASH hátrányosan befolyásolhatja a betegek életminőségét; azonban a NASH kezelésére még nem engedélyezett gyógyszerek vagy terápiák.
Egy nemrégiben, a New England Journal of Medicine (NEJM) című folyóiratban megjelent tanulmány (ENLIVEN) kimutatta, hogy a pegozafermin javította mind a májfibrózist, mind a májgyulladást biopsziával igazolt, nem cirrózisos NASH-betegeknél.
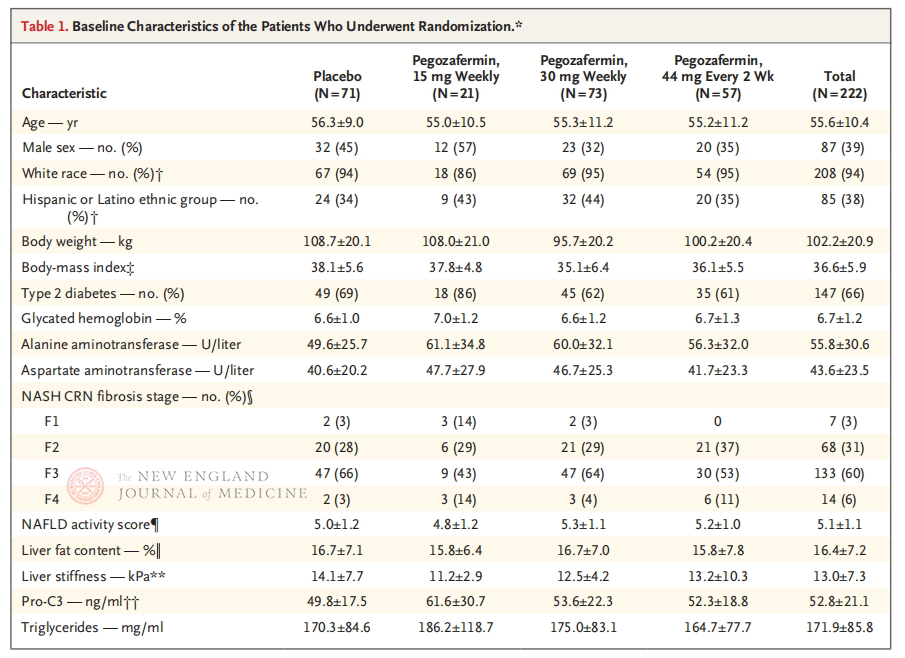
A Rohit Loomba professzor és klinikai csapata által a San Diegó-i Kaliforniai Egyetem Orvostudományi Karán végzett multicentrikus, randomizált, kettős vak, placebo-kontrollos, IIb fázisú klinikai vizsgálatot 222, biopsziával igazolt F2-3 stádiumú NASH-ban szenvedő beteg vett részt 2021. szeptember 28. és 2022. augusztus 15. között. A betegeket véletlenszerűen osztották be pegozafermin (szubkután injekció, hetente egyszer 15 mg vagy 30 mg, vagy kéthetente egyszer 44 mg) vagy placebo (hetente egyszer vagy kéthetente egyszer) csoportba. Az elsődleges végpontok közé tartozott a fibrózis ≥ 1. stádiumú javulása és a NASH progressziójának hiánya. A NASH fibrotikus progresszió nélkül megszűnt. A vizsgálat biztonságossági értékelést is végzett.
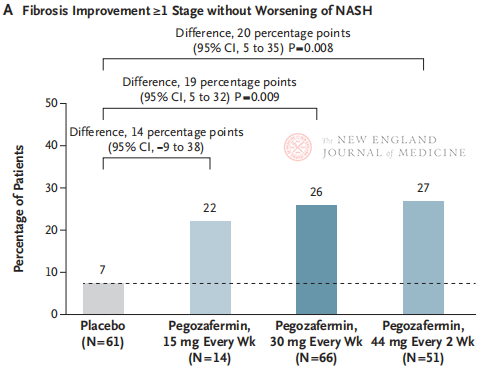
24 hetes kezelés után a fibrózisban ≥ 1. stádiumú javulást mutató és a NASH rosszabbodását nem mutató betegek aránya, valamint a NASH regresszióját mutató és a fibrózis rosszabbodását nem mutató betegek aránya szignifikánsan magasabb volt a három Pegozafermin dóziscsoportban, mint a placebo csoportban, és a kéthetente egyszer 44 mg-mal vagy a hetente egyszer 30 mg-mal kezelt betegeknél szignifikánsabb különbségeket mutattak. Biztonságosság szempontjából a pegozafermin hasonló volt a placebóhoz. A pegozafermin-kezeléssel kapcsolatos leggyakoribb mellékhatások a hányinger, a hasmenés és az injekció beadásának helyén fellépő bőrpír voltak. Ebben a IIb fázisú vizsgálatban az előzetes eredmények arra utalnak, hogy a pegozaferminnel végzett kezelés javítja a májfibrózist.
A vizsgálatban alkalmazott pegozafermin a humán fibroblaszt növekedési faktor 21 (FGF21) hosszú hatástartamú glikolált analógja. Az FGF21 egy endogén metabolikus hormon, amelyet a máj választ ki, és szerepet játszik a lipid- és glükózanyagcsere szabályozásában. Korábbi tanulmányok kimutatták, hogy az FGF21 terápiás hatással van a NASH-betegekre azáltal, hogy növeli a máj inzulinérzékenységét, serkenti a zsírsav-oxidációt és gátolja a lipogenézist. A természetes FGF21 rövid felezési ideje (kb. 2 óra) azonban korlátozza a NASH klinikai kezelésében való alkalmazását. A pegozafermin glikozilált pegilációs technológiát alkalmaz a természetes FGF21 felezési idejének meghosszabbítására és biológiai aktivitásának optimalizálására.
A jelenlegi IIb fázisú klinikai vizsgálat pozitív eredményei mellett egy másik, a Nature Medicine folyóiratban (ENTRIGUE) megjelent tanulmány kimutatta, hogy a pegozafermin jelentősen csökkentette a trigliceridek, a nem HDL-koleszterin, az apolipoprotein B és a májzsírosodás szintjét súlyos hipertrigliceridémiában szenvedő betegeknél, ami pozitív hatással lehet a szív- és érrendszeri események kockázatának csökkentésére NASH-ban szenvedő betegeknél.
Ezek a tanulmányok arra utalnak, hogy a pegozafermin, mint endogén metabolikus hormon, számos metabolikus előnnyel járhat a NASH-ban szenvedő betegek számára, különösen azért, mert a NASH-t a jövőben esetleg metabolikusan összefüggő zsírmájbetegségnek nevezik át. Ezek az eredmények nagyon fontos potenciális gyógyszerré teszik a NASH kezelésében. Ugyanakkor ezek a pozitív vizsgálati eredmények támogatni fogják a pegozafermin bevonását a 3. fázisú klinikai vizsgálatokba.
Bár mind a kéthetente 44 mg-os, mind a heti 30 mg-os pegozafermin kezelés elérte a vizsgálat szövettani elsődleges végpontját, a kezelés időtartama ebben a vizsgálatban mindössze 24 hét volt, a placebo csoportban a betegek együttműködési aránya pedig mindössze 7% volt, ami szignifikánsan alacsonyabb volt a korábbi, 48 hétig tartó klinikai vizsgálatok eredményeinél. Ugyanazok a különbségek és a biztonságosság? A NASH heterogenitása miatt a jövőben nagyobb, többközpontú, nemzetközi klinikai vizsgálatokra van szükség, amelyek nagyobb betegpopulációt vonnak be, és meghosszabbítják a kezelés időtartamát a gyógyszer hatékonyságának és biztonságosságának jobb értékelése érdekében.
Közzététel ideje: 2023. szeptember 16.